文章图片

加拿大杨梅生物制药公司(Arbutus Biopharma Corporation)的首席开发官 , Gaston Picchio博士在最近一次科学会议上(在新加坡举行的“治愈HBV”为主题)更新了乙肝创新药研发管道进展 , 包含一种衣壳抑制剂AB-836 , 目前正在开发用于治疗慢性HBV感染的临床试验 。
最近一次科学会议 , Arbutus Bio首席开发官比较了下一代衣壳抑制剂AB-836和第一代衣壳抑制剂AB-506乙肝在研新药AB-836 , 1a/1b期已基本完成 , 下一代核心抑制剂
目前 , AB-836正在第1期临床试验后部分的扫尾阶段 。 在新加坡举行的科学会议上 , Gaston Picchio博士介绍 , 与前一代衣壳抑制剂相比(指AB-506) , AB-836具有提高功效和增强耐药性的潜力 。
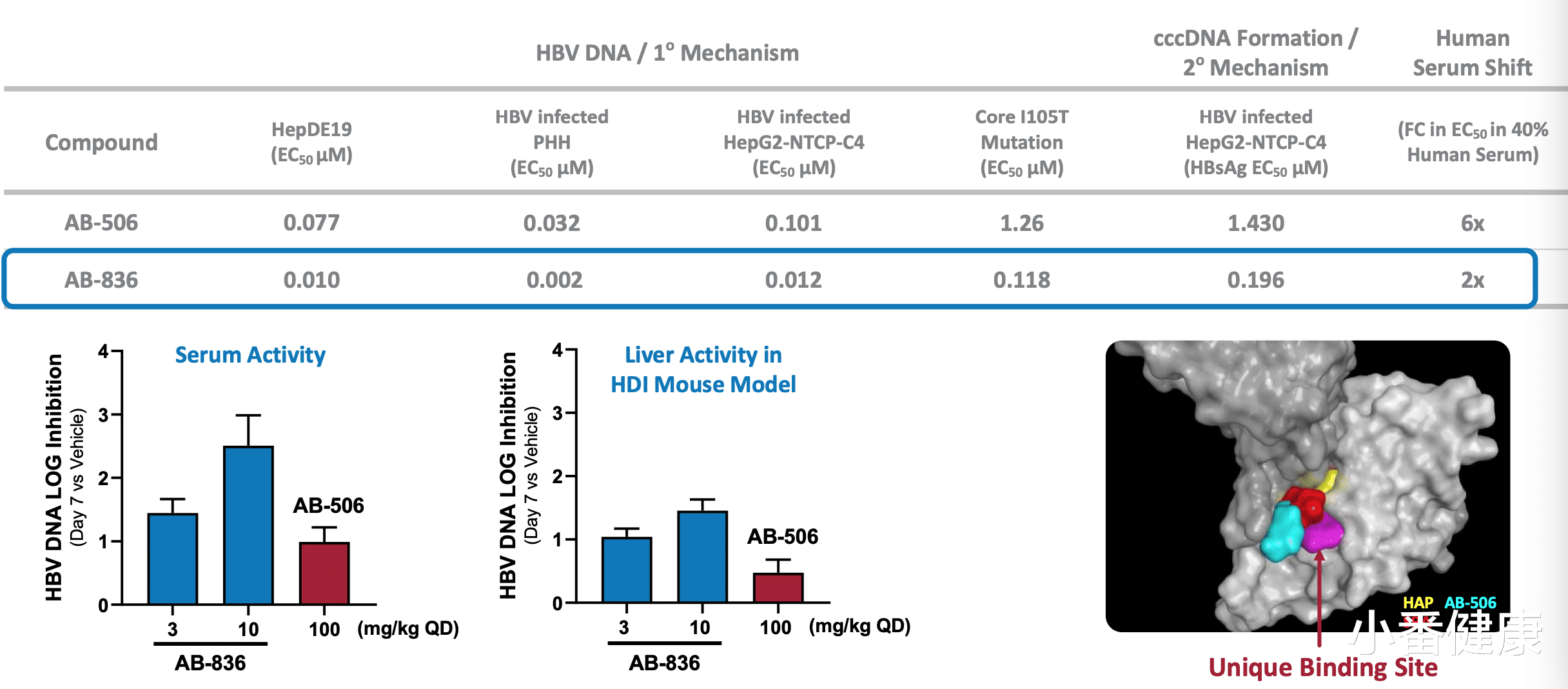
AB-836不同于 AB-506 和 II类衣壳抑制剂领域的其他竞争化合物的新型化学系列 。 AB-836利用核心蛋白二聚体-二聚体界面内的新结合位点 , 具有 EC50 < 10 nM提高的内在效力 , 对核苷(酸)类似物(NA)耐药变异有效;解决了已知衣壳抗性变体 T33N 和 I105T 的潜力;
同时 , AB-836还提供了低剂量和宽治疗窗口的潜力 , 在多个物种中表现出高肝脏浓度 。 AB-836可每日给药一次 , 具有泛HBV基因型特点 , 可与其他MOA代理疗法组合使用 。
AB-836-001研究是一项1a/1b期临床试验 , 该试验第1部分是在健康受试者的单次递增剂量;第2部分是在健康受试者的多次递增剂量;第3部分是针对慢性乙肝受试者的多剂量给药 , 该试验展开的初步数据及核心结论如下:
第1部分和第2部分 , 主要在健康受试者中的单剂量和多剂量使用乙肝候选药物AB-836;第3部分用于cHBV患者 , 按 50毫克和100毫克 AB-836 每日一次给药 , 持续28天 。
1期1-2部分安全性结果:没有死亡或发生严重不良事件(SAEs);出现1名受试者(每日50毫克)因躁动AE在第13天停药;除发现3例不良事件(AEs)外 , 所有 AEs 均为轻度(2级头痛、躁动和支气管炎) , 1例评估为药物相关(1级皮疹) 。 在临床实验室检查、心电图、生命体征或身体检查中 , 未发现有临床意义的明显异常 。
1期第3部分结果:没有出现死亡或不良事件;1名受试者出现 ALT 从基线 1级 到 3级 的短暂升高 , 持续给药后缓解;心电图、生命体征或体格检查均无临床异常 。 疗效评估(在队列G-100毫克 QD):提供强大的抗病毒活性- 在第28天(n=4)时 , 平均(SE)较基线 -3.1 log (0.5)变化 。
【乙肝在研新药AB-836,1a/1b期已基本完成,下一代核心抑制剂】小番健康结语:最近 , 在新加坡举行的以“治愈HBV”为主题的科学会议上 , Arbutus公司的Gaston Picchio博士介绍了下一代乙肝病毒衣壳抑制剂AB-836的最新开发进展并将化学结构、作用机制拿来与早期研发的一款衣壳抑制剂AB-506进行比较 。 目前 , AB-836的第1a/1b期临床开发已基本完成 。
推荐阅读
- 乙肝在研新药OLX703A,2023年进临床试验,NASVAC正在日本研究中
- 乙肝CAMs化合物,部分早期动物实验实现HBsAg丢失,正在寻找原因
- 乙肝药物研发,REP301/401研究公布,NAPs成功确认对SVP靶向能力
- 关心乙肝创新药时,丁肝药物格局已改变,简述Lonafarnib多项进展
- 老杜遇到麻烦!被怀疑没在药房生育,网友建议公开两个证据正视听
- 乙肝药物发现,基于RG-7834衍生物,可减少HBsAg兼具肝靶向性
- 医生 2013年,医生以“患病”为由拐卖婴儿,产妇再次检查身体明白被骗
- 乙肝 乙肝美肝会前夕,先认识部分新靶点,以及主要作用机理
- 蛋白质 乙肝检查点抑制剂,介绍作用机理,本质上都属于人工蛋白质


