*仅供医学专业人士阅读参考
本文图片
自分泌PD-1抗体+CAR-T治疗 , 晚期卵巢癌的“杀手”!
自2018年的诺贝尔生理学和医学奖获得者日本免疫学家Tasuku Honjo发现了PD-1分子对免疫反应的抑制机制之后 , PD-1抑制剂应运而生 。 PD-1抑制剂在多个瘤种尤其是非小细胞肺癌(NSCLC)领域均可谓是“战功显赫” , 给无数肿瘤患者带去新生 。
【肿瘤|厉害了!快来看看这种“黑科技”是如何打败“最凶妇癌”的丨病例小课堂】如果说包括PD-1抑制剂在内的免疫检查点抑制剂是人类在免疫治疗时代打响的第一场战斗 , 那么CAR-T治疗则是基于新理念、新技术、新手段的另一座里程碑 。 CAR-T治疗在血液肿瘤领域中的疗效和安全性已经被认可 , 第一个五年随访数据也于近日发表 。
令人振奋的是 , 中国学者已经对以上两种治疗方式进行了强强联合的尝试 , 但这种联合疗法并不是单纯的PD-1单抗与CAR-T治疗联用 , 而是自分泌PD-1抗体的CAR-T细胞联合疗法(αPD-1-mesoCAR-T) 。
上海市第十人民医院许青教授临床团队与上海细胞治疗集团钱其军教授科研团队近日就在Journal for ImmunoTherapy of Cancer上发表了一个该创新疗法成功救治的晚期卵巢癌病例 。 “医学界肿瘤频道”诚邀许青教授为广大读者详解此项成果 。
打开实体瘤CAR-T治疗之“锁”
在介绍该病例之前 , 我们先将目光聚焦于该病例使用的创新组合疗法的诞生之路 。 虽然刚刚介绍过CAR-T治疗在血液肿瘤领域中的显著成果 , 但CAR-T治疗在实体瘤领域中的应用仍挑战重重:免疫相关副反应以及治疗后的复发仍是其所面临的主要问题 , 并且实体瘤表面用于特异性识别抗原的缺乏与肿瘤微环境的抑制也是需要解决的问题 。
许青教授表示:
由于实体瘤理想的肿瘤特异性抗原很少 , CAR-T细胞治疗反应不容乐观 。 间皮素(Mesothelin , MSLN)是一种分化抗原 , 在卵巢癌中高表达 , 但在正常组织中低表达 , 并且通常与晚期卵巢上皮癌(EOC)的化疗耐药性和不良预后相关 。 我们之前的研究得出靶向间皮素-T细胞显著抑制MSLN阳性卵巢癌在体外和体内的生长这样的结果 。
并且在该病例的诊治中 , 我们还加入了多靶点血管生成抑制剂阿帕替尼 , 该药对肿瘤微环境的改变也对整体的联合疗法起到了非常重要的奠定和推动作用 。 因此 , 就‘诞生’了这样一种自分泌PD-1抗体MSLN靶向CAR-T细胞免疫疗法+阿帕替尼的组合疗法 。
病例一览
病史简介:54岁女性 , 诊断为IIIc期晚期卵巢浆液性腺癌 , 于2015年9月接受了肿瘤切除术 。
辅助检查:肿瘤组织的免疫组化染色显示CK7(+)、CA125(+)、WT-1(+)、EMA(+)、CAM5.2(+)、ER(+)、PR(+++)、Calretin(部分+)、p53(+++)、Ki67(60%)、CD34(血管+)阳性 , HER2、CK20、CA19-9、波形蛋白、CEA和HBME-1阴性 。 左输卵管染色也有相同的病理特征 。
治疗经过:
1.先用紫杉醇联合顺铂一线化疗8个周期 , 后用吉西他滨联合奥沙利铂二线化疗4个周期 。 患者病情稳定(SD) 。
2.2017年8月 , MRI检查显示在她的肝脏发现新的病变 。 然后 , 阿霉素脂质体联合奈达铂给药6个周期 。
3.2018年3月 , 随着肝脏病变的扩大 , 出现CA125升高 , 并给予阿帕替尼(250 mg/天 , 口服) 。 治疗后CA125下降(图1A) , 患者达到8个月的SD 。
4.2018年10月 , CA125升高 。 患者要求免疫治疗 。 经确认 , MRI在肝脏有两个可测量的结节(图1B) , 在肺和盆腔区域未发现转移病灶 。 四种错配修复蛋白(MLH1、MSH2、MSH6和PMS2)正常表达 , 微卫星稳定 , 19个与肿瘤发生相关的常见基因也未发现突变 。 然而 , MSLN(++84%)在她的肿瘤组织中染色很强(图2) , 因此患者接受参加αPD-1-mesoCAR-T细胞治疗的临床试验 。 患者在开始单采前签署了知情同意书 。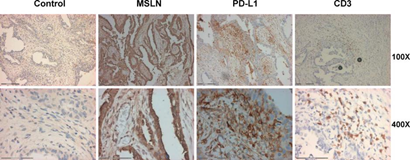
本文图片
图1.卵巢癌组织MSLN、PD-L1和CD3表达的免疫组化分析
5.2018年12月 , 开始首次输注CAR-T , 2019年1月开始第二次输注 。
临床反应:研究者对患者的CA125水平进行监测:曲线从服用阿帕替尼的第一天开始到免疫治疗观察期结束 , 第2个月下降 , 第8个月上升 。 两次的CAR-T细胞治疗使其在2个月的治疗中下降 。 如图2A所示 , CA125在第一次输注CAR-T细胞后略有下降 。 虽然在第二次输注后再次升高 , 但没有超过第一次CAR-T治疗前的水平 。
右肝叶两个转移灶联合免疫治疗后 , N1直径由51.9毫米降至39.1毫米 , N2直径由19.4毫米降至无法检测(图2B、C) 。 患者获得获得部分缓解(PR) 。 患者无进展生存期(PFS)5个月 , 存活17个月 。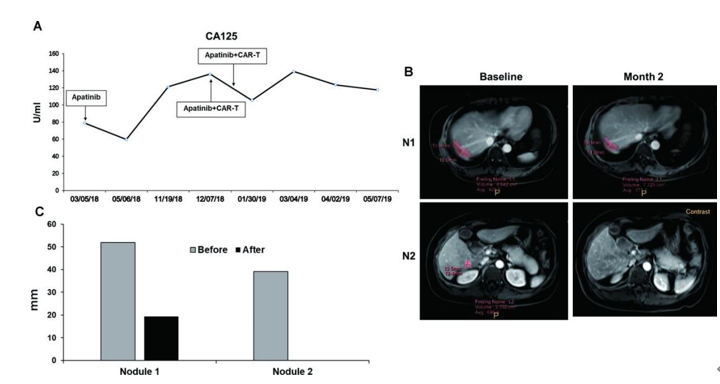
本文图片
图2.患者的临床反应
在本研究中 , 患者在第0天和第26天通过静脉滴注接受αPD-1-mesoCAR-T细胞(图3A) 。 第0天 , CAR-T产品的拷贝数为25.4拷贝数/μg DNA 。 第一次输注后的第5天为85.5拷贝数/μg DNA , 第二次输注后达到峰值(198拷贝数/μg DNA) 。 在第31天 , 它下降到46.1拷贝数/μg DNA 。 PD-1抗体的水平在输注后也升高并维持在恒定水平 , 支持αPD-1-mesoCAR-T细胞可以在体内扩增 。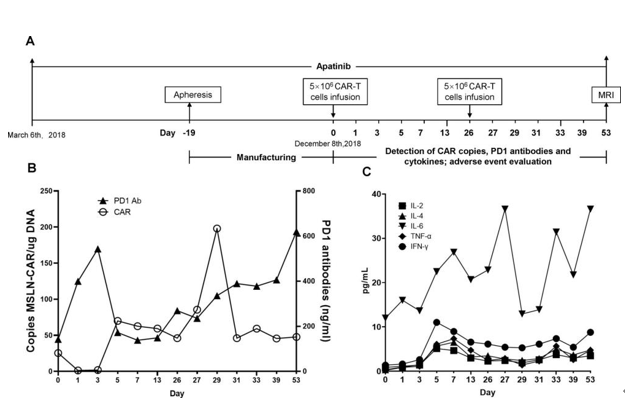
本文图片
图3.患者治疗期间输注和扩增CAR-T细胞及PD-1抗体和细胞因子水平
组合疗法或成晚期卵巢癌“破局之道”?
晚期卵巢癌作为女性杀手之首 , αPD-1-mesoCAR-T细胞疗法的突破和前景无疑是为卵巢癌的治疗注入了“新鲜力量” 。 而细究该疗法取得成功背后的原因 , 则又给了临床医生以全新的启示和方向 。
许青教授介绍道:
这个成功救治的晚期卵巢癌病例可以说是给未来的卵巢癌治疗提供了一个新模式或者说是一个方向 。 晚期卵巢癌的治疗 , 特别是前期治疗失败、效果不理想这类患者可能还是需要这样一个联合治疗的模式来延长生存期和提高生存质量 。
就像我们这个病例所提示的:在抗血管形成治疗改善肿瘤微环境 , 为下一步的治疗打下基础;靶向MSLN的精准CAR-T细胞治疗再联合自分泌PD-1抗体更能增强杀伤力 , 巩固疗效 。 这样一种联合模式也许就能够扭转晚期卵巢癌治疗颓势 , 使更多患者获益 。
实体瘤CAR-T细胞治疗的未来之路
αPD-1-mesoCAR T细胞治疗为晚期难治性卵巢癌提供了一种有前途的免疫治疗方法 , 给未来的实体瘤CAR-T细胞治疗开了个好头 , 值得进一步的临床试验 。 这项研究的局限性在于测量缩小的肿瘤组织中CAR-T细胞的扩增和PD-1抗体的浓度 。 此外 , 还需要更多的患者来验证目前病例中观察到的临床反应 。
许青教授补充道:
除了病例中提到得晚期卵巢癌 , 我们也对原发性肝癌、具有高危预后的早期结肠癌、胸膜间皮瘤和腹膜间皮瘤的患者进行了对应的临床试验 。 目前我也可以向大家透露:有一例患者已经达到了完全缓解(CR) 。 这些成果都提示着临床医生:在某些特定实体瘤中 , 尤其是无法从传统治疗中获益的患者 , CAR-T治疗也许就能够带来新希望 。
除了以上所介绍的CAR-T细胞治疗相关的研究 , 我们研究团队针对其它类型的免疫治疗以及联合治疗也进行了不断地探索 , 比如溶瘤病毒联合PD-1抗体治疗晚期结肠癌肝转移的临床试验、肿瘤浸润淋巴细胞疗法(TIL)等等 。 并且针对精准治疗 , 我们团队也做了大量的工作和努力 , 包括探索更多潜在生物标志物比如通过肠道菌群来筛选患者 , 利用人工智能(AI)技术来辅助判断免疫治疗疗效 。 未来我们也将进行更多的探索和尝试 。
相信随着科学家对肿瘤以及人体免疫系统机制越来越多的揭示 , 更多类型的免疫治疗会横空出世 , 碰撞出更加精彩的火花!
专家简介
本文图片
许青教授
主任医师、教授、医学博士、博士生导师、留美博士后、上海市浦江人才
同济大学附属上海市第十人民医院肿瘤科主任、肿瘤学教研室主任、GCP肿瘤学负责人
同济大学癌症中心常务副主任
中国医药生物技术协会副理事长
中国医药教育协会盆腔肿瘤专业委员会主任委员、肿瘤转移专业委员会候任主任委员
中国临床肿瘤学会(CSCO)理事、智慧医疗专业委员会常委、泌尿与男性生殖系统肿瘤专业委员会委员、免疫治疗专业委员会委员
上海市抗癌协会理事、肿瘤免疫治疗专业委员会候任主任委员、疑难肿瘤专业委员会副主任委员、恶性黑色素瘤专业委员会副主任委员、姑息与康复治疗专业委员会常委 。
中国中药协会肿瘤药物研究专业委员会副主任委员
参考文献:
[1].Fang J,Ding N,Guo X,et alαPD-1-mesoCAR-T cells partially inhibit the growth of advanced/refractory ovarian cancer in a patient along with daily apatinibJournal for ImmunoTherapy of Cancer 2021;9:e001162.doi:10.1136/jitc-2020-001162
本文首发:医学界肿瘤频道
本文作者:uu
本文审核:许青教授
责任编辑:Sharon
推荐阅读
- 骁龙|骁龙8旗舰驯龙大战一触即发,“大师”和“高手”谁更厉害?
- Apple|竞争对手挖墙角太厉害 苹果以18万美元特别股票奖励慰留工程师
- 每日经济新闻|港大深圳医院院长卢宠茂:“港澳药械通”政策下肿瘤治疗所用药械急需引进
- 团队|厉害!华中农大团队找到控制鱼刺基因
- 肿瘤患者|肿瘤患者CAR-T治疗援助计划在沪落地
- 李钦|肿瘤患者CAR-T治疗援助计划在沪落地
- 肿瘤|变老你怕吗?中国团队发现突破性“抗衰老”物质!
- 人物|“球王”贝利再次入院接受治疗 因结肠肿瘤:预计几日后可出院
- 阿尔茨海默|“伟哥”真厉害?华裔科学家:在预防老年痴呆症上或有显著功效
- 团队|顶级厉害的年轻人,都在做些什么?




